脂質的消化過程始于唾液分泌、咀嚼以及舌脂酶在口腔中的釋放。當消化物進入胃部時,舌脂酶從舌部漿液腺釋放后,會通過水解甘油三酯結構中sn-3位點的游離脂肪酸來完成后續分解,其中“sn”表示甘油骨架的立體化學編號方式。進入胃部后,胃脂肪酶繼續水解脂質,主要釋放出原本作為甘油三酯成分的短鏈脂肪酸。盡管這兩種脂肪酶都參與了水解作用,但進入十二指腸上段的脂質中仍有超過70%是甘油三酯。因此,小腸才是脂質消化的主要場所。

小腸中脂質的消化過程主要依賴兩大關鍵成分:膽汁酸和胰脂肪酶。膽汁酸由肝臟中的膽固醇轉化生成,隨后被濃縮儲存于膽囊。當循環系統中膽囊收縮素(一種肽類激素)水平升高時,就會引發水油乳化現象,從而促使膽汁酸釋放至腸道腔內。盡管膽汁酸對于微膠束的形成至關重要,但當其被釋放入腸腔時,最初會抑制胰腺脂肪酶的活性。這種抑制是由于膽汁酸物理性地阻止胰腺脂肪酶與腸腔中的脂滴接觸。共脂肪酶通過結合胰腺脂肪酶來逆轉膽汁酸的抑制作用,兩者一旦結合后便能附著于脂滴表面。當胰腺脂肪酶通過共脂肪酶的結合作用附著于脂滴后,便會酶促催化甘油三酯中sn-1和sn-3位的酯鍵斷裂。該酶促水解反應生成兩個游離脂肪酸以及一個在sn-2位酯化脂肪酸的單甘酯。此酶促反應速率極快,其產生游離脂肪酸和單甘酯的速度遠快于后續微膠束的整合速度。而抗胰腺脂肪酶水解的磷脂則通過磷脂酶A2進行消化。磷脂酶A2通過酶促反應從sn-2位釋放脂肪酸,產生溶血磷脂和游離脂肪酸。共脂肪酶將新水解的產物從腸腔中的脂滴運輸至正在形成的含膽汁酸鹽的微膠束中。
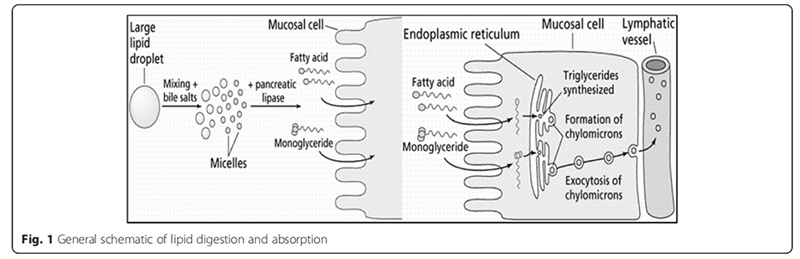
膽汁中的脂質物質會形成膠束結構。這種結構的形成源于膽囊分泌的膽汁酸與磷脂共同作用:膽汁酸的一端朝向消化物和腸腔的水環境,另一端則指向膠束中心。通過這種特殊取向,膽汁酸與磷脂在膠束中形成了疏水核心和親水邊緣的結構特征。研究表明,當脂質被整合到膠束結構時,其對多不飽和脂肪酸(PUFA)和飽和單酰基甘油酯表現出更強的結合能力。混合膠束一旦形成,就會穿過腸腔直達腸上皮細胞的靜水層。這種膠束結構巧妙解決了脂質在腸道水環境中易受疏水性影響的問題,不僅讓脂質能輕松穿透靜水層,還能使腸上皮吸收表面附近的游離脂肪酸、單甘酯等脂質物質濃度提升100至1000倍。圖1簡明展示了脂質消化與吸收的完整過程。
由于膠束中脂質物質的富集形成了濃度梯度,脂質成分可通過非能量依賴的過程被動擴散進入腸細胞。當腸腔內脂質含量較低時,也有證據表明存在依賴載體的脂質雙層吸收過程。這種雙重機制在理論上被提出用于維持膳食脂質攝入量低時必需脂肪酸的必要水平,但尚不清楚當膳食脂質攝入正常或較高時載體介導的運輸是否重要。由于腸道的攪動作用和結構特征,膠束之間保持著動態平衡關系,這使得上皮細胞、膠束和脂滴幾乎持續接觸。這種高度接觸將脂質成分從高密度膠束分配到低密度膠束。這種分配使膠束均勻獲取并分布脂質成分,最終意味著小腸腔內脂質消化的限制因素是膠束飽和度。脂質成分從膠束穿越靜水層的穿梭過程是一種鏈式反應,其依賴于腸細胞處脂質的低濃度。腸道脂肪酸結合蛋白通過結合游離脂肪酸,并將其截留在頂膜區域,從而促進脂肪酸的吸收。膽汁酸可在回腸末端被高效重吸收,繼而轉運至肝臟循環利用,參與后續的脂質消化過程。
當脂肪酸(FA)擴散至腸細胞后,會通過甘油-3-磷酸途徑或單酰基甘油途徑在內質網中重新酯化。經過甘油三酯的再酯化過程后,多個甘油三酯和膽固醇酯會被包裝成乳糜微粒。乳糜微粒含有80%至95 %的甘油三酯、2%至7%的膽固醇以及3%至9%的磷脂。其外層由磷脂雙分子層和載脂蛋白構成,這些成分能增強溶解度并提高酶識別能力。隨后,乳糜微粒通過胸導管進入淋巴系統,最終進入血液循環系統。
乳糜微粒進入血液循環后,既可儲存在脂肪細胞中,也可被肌纖維等細胞氧化分解。當胰島素和合成代謝激素水平升高時,這些微粒就會被轉運至脂肪細胞進行儲存。這一過程主要受胰島素對脂肪細胞脂蛋白脂肪酶的刺激作用調控,而肌肉細胞中的脂蛋白脂肪酶同工酶則不受胰島素影響。因此,多功能酶脂蛋白脂肪酶會在脂肪細胞的毛細血管腔內表達,專門負責處理富含甘油三酯的乳糜微粒及其他脂蛋白。脂肪酸會以被動擴散方式逐個進入細胞,隨后在脂肪細胞內重新酯化形成甘油三酯儲存。
與含有16至20個碳原子脂肪酸的長鏈甘油三酯不同,中鏈甘油三酯主要由含有8和10個碳原子的飽和脂肪酸構成。當這些脂肪酸被脂肪酶快速分解后,即使在少量腔內膽汁酸和胰脂肪酶存在的情況下,它們仍具有高水溶性,能迅速被黏膜細胞吸收形成乳糜微粒。隨后,這些中鏈脂肪酸與白蛋白結合,通過門靜脈系統運輸至肝臟,并以不依賴肉堿的方式進入線粒體進行后續氧化反應。